来源:百小蓁发布时间:2023-06-09浏览量:332次
抗体是人体免疫系统中最重要的分子。在上个世纪,由于IgGs在抗传染病方面的作用,受到了深入研究,并在过去十年中占据了治疗学发展的中心舞台。除了感染性疾病,重组抗体现在也被用于癌症、风湿性关节炎和各种其他病理状况作为人体防御机制的关键物质,治疗性和内源性体液抗体鉴定的关键步骤是确定氨基酸序列。到目前为止,这一任务主要是通过在核苷酸水平上对B细胞受体(BCR)库进行测序来解决的。近年来质谱(MS)已经成为在相关的蛋白质水平上获得序列信息的直接替代工具。虽然现在已经建立了几种质谱分析方法,但重组抗体和内源性抗体的分析仍面临着一系列特殊的挑战,需要超越传统蛋白质组学工作流程的方法。
01
质谱在抗体发现中的新作用
由于抗体结构的复杂性和序列多样性,治疗性抗体的开发一直是一项极具挑战性的任务。抗体发现的策略包括筛选感染个体中B细胞,将外周血单个核细胞(PBMCs)分离、永生化、筛选抗原反应性。进一步对反应性克隆进行扩增和表征,有效地找到新的中和抗体。最新进展表明该策略可以用于某些传染病的抗体开发,如埃博拉或严重急性呼吸综合征冠状病毒2(SARS-CoV-2)等。然而,直接从临床样本的蛋白质水平上发现和表征功能成熟且具有活性的成熟抗体克隆可能更为有利。近年来,基于质谱的蛋白质组学在样品制备、质谱和液相色谱仪器、数据分析等方面取得了巨大进展,用质谱进行蛋白质水平的抗体测序极具潜力。目前已有三种主要基于质谱的策略用于确定抗体序列(图1)。第一种策略适用于高度纯化的重组抗体,这些抗体可以利用自下而上(BU-MS)方法,通过结合几种不同的蛋白酶和先进的算法进行全测序;第二种通过结合基于质谱的技术和基因组学/转录组学的方法分析内源性抗体,例如全基因组测序或BCR测序生成个性化序列数据库,将BU-MS数据基于此数据库搜索;第三种包括多种基于质谱的从头测序方法,实现不借助替代组学数据,直接从临床样本中确定选定克隆的完整抗体序列。
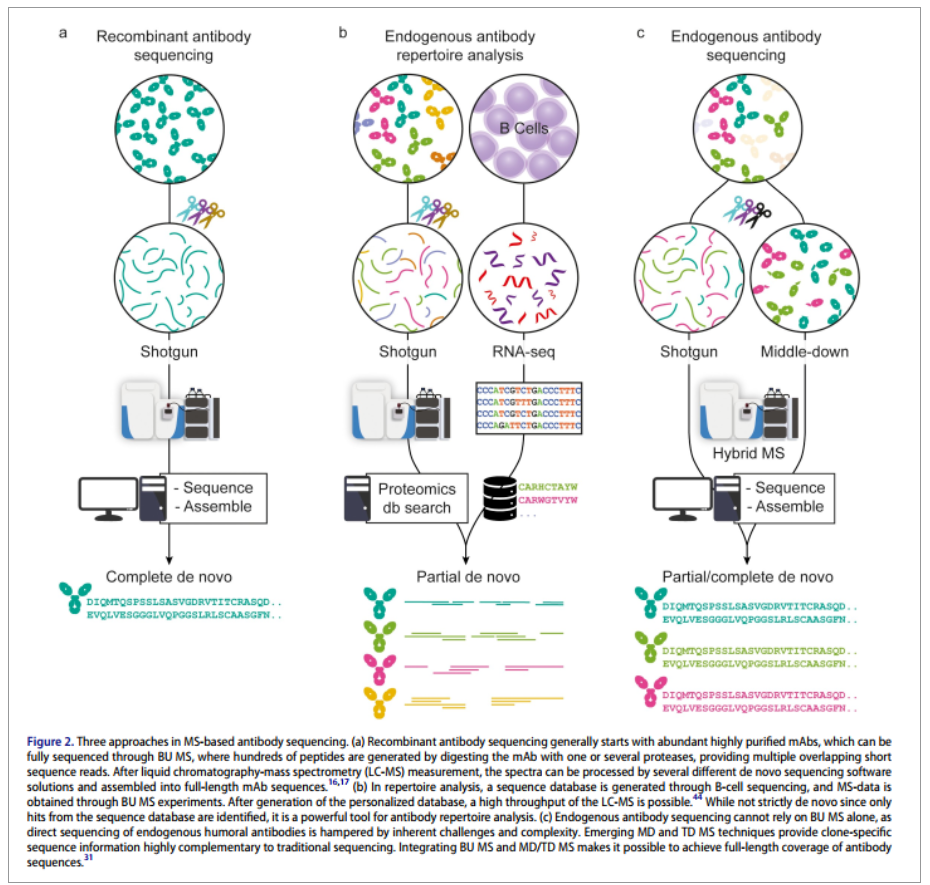
图1:基于质谱的三种抗体测序方法
02
基于质谱的单克隆抗体分析方法
蛋白质组学是对蛋白质的大规模研究,许多以不同肽和蛋白质为中心的质谱方法已开发用于蛋白质组学,其中一些已适用于抗体的从头序列分析。BU-MS方法是迄今为止在质谱蛋白质分析中最广泛的方法。酶消化和质谱裂解遵循高度特定的规则,可以获得多肽及其片段离子,产生重叠多肽并完全序列覆盖,从而获得抗体序列,如图2所示。为了获得完整和准确的抗体序列,通常需要协同序列特异性的多种蛋白酶酶切以及互补的质谱离子碎裂技术,此外同源数据库辅助搜索也是抗体从头测序的关键,但值得注意的是,传统的数据库搜索即使在最广泛的数据库中,也可能不存在与目标序列的精确匹配,因此,同源辅助方法需基于序列比对或子序列(即序列标签)提取的容错片段匹配算法,可以使用同源数据库匹配的序列对实验确定的序列进行评分,目前有多种软件可用于抗体从头测序,如PEAKS AB软件,这些软件可以利用多种酶解、多重片段化方法产生的数据以及使用同源抗体序列数据库的优势,对蛋白样品进行完整的从头序列预测。
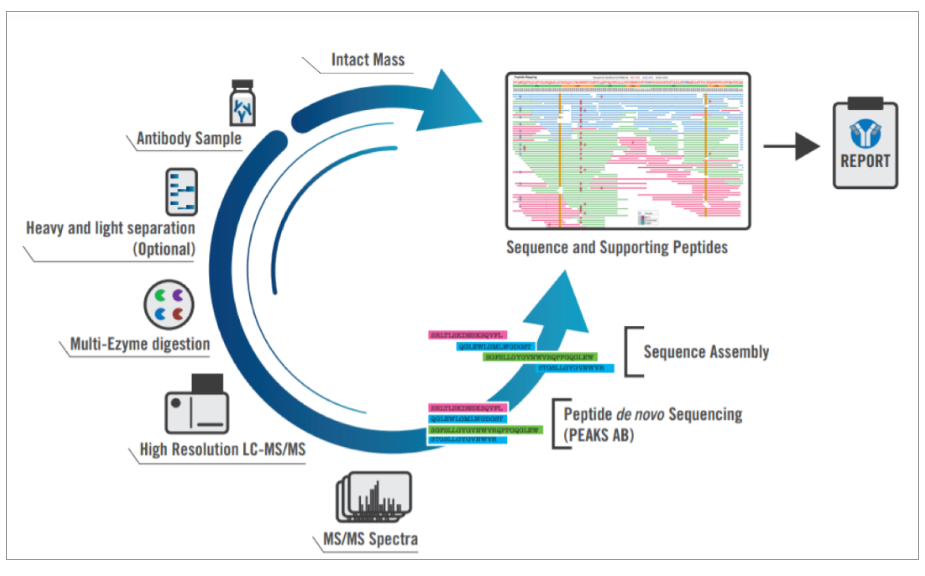
图2:抗体测序流程图
03
基于质谱的多克隆抗体测序
对整个血清抗体库进行从头测序是极具挑战性的,第一个障碍是样本的可用性,多克隆抗体样本通常来自临床样本,因此只能获得有限的数量。此外血浆中单克隆的浓度约为1 μg/mL,分离单个克隆抗体极具挑战性,进一步复杂了测序过程,而大多数软件工具是专门为组装单个抗体而设计的,因此当数据中多个相似的IgG序列时,无法进一步分析。第二个障碍是在复杂的内源性多克隆抗体混合物中,由于稀释效应,高可变区域的关键序列信号往往无法检测到,来自保守区域的序列信号被放大(因为后者存在于每个单克隆中),从而抑制了每个单克隆唯一的CDRs信号。而质谱方法的发展以及生信软件的开发,目前完整蛋白质的LC-MS能够从复杂的抗体混合物中检测和分析单个克隆,此外,使用混合或多组学策略也有助于多克隆抗体分析(图1b)。例如,Bondt等人发现每个供体有50-500个持续存在的IgG1 Fab克隆,而每个供体的IgG1基因库都表现出简单独特的克隆体库且量大的克隆体仅有几百个。所以他们设法在不用抗原特异性捕获的情况下,利用从国际免疫遗传学信息系统(IMGT)数据库中选择与轻链和重链紧密匹配的种系模板,结合多种蛋白酶消化和ETD采集的BU MS数据,利用数据迭代完善这些模板,产生最终的成熟序列,直接对患者血液中高丰度的克隆进行从头测序(图3)。
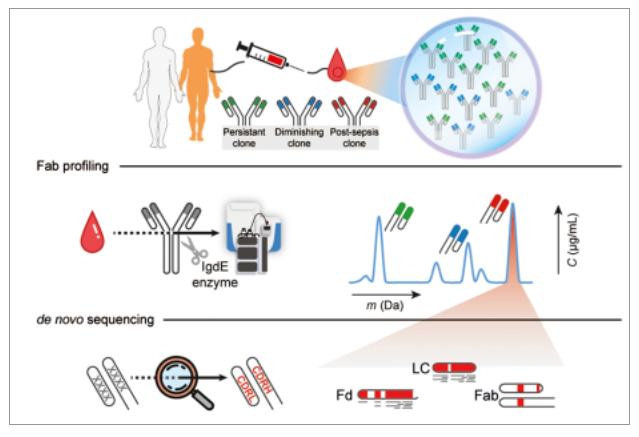
图3. 以质谱为基础的血清抗体的从头测序
04
从头测序发现的治疗性抗体的发展
过去十年在基于质谱的抗体测序方面取得的进展为未来的发展提供了乐观的前景。自20世纪60年代以来,抗体的样品制备初步形成,但获得序列信息的实用方法直到1993年Sanger测序首次应用于B细胞时才出现,到2008年下一代测序导致了高通量测序工作流程,并进一步促进了治疗性抗体的开发,随后,基于质谱的蛋白质组学的普及进一步促进了抗体从头测序平台的发展,自那以来抗体序列和注册的抗体疗法的数量一直呈指数级增长 (图4)。
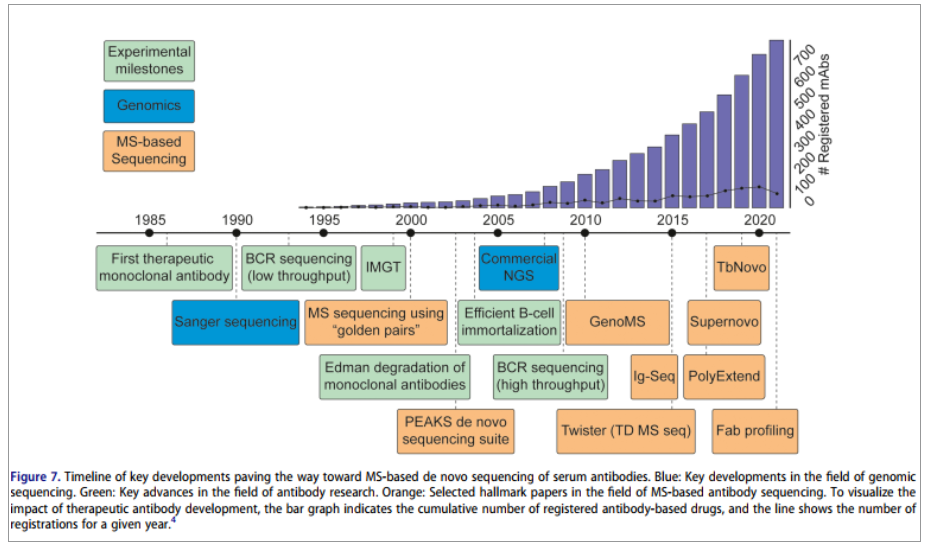
图4:抗体从头测序的关键发展时间表(蓝色:基因组测序领域的关键进展;绿色:抗体研究领域的关键进展;橙色:在质谱抗体测序领域的代表性论文;条形图表示基于抗体的药物注册的累积数量,线条表示给定年份的注册数量)
小编总结:
本文总结了质谱在抗体发现的应用与发展,以及基于质谱的蛋白质组学的最先进的方法。随着高精度质谱仪的出现,软件系统的不断更新,基于质谱的抗体从头测序相关的瓶颈正在一步步突破,通过多种蛋白酶、多重片段技术、同源性数据库辅助测序的策略,已完全实现单克隆抗体、重组单克隆抗体的完整测序。尽管不能直接应用于血清中内源性抗体混合物的分析,但与其他蛋白质基因组学结合的策略也可实现多克隆测序的部分测序。
百蓁生物拥有BSI 授权的质谱抗体测序技术、自主知识产权的PEAKS系列分析软件和经验丰富的专业技术服务团队,是抗体(蛋白)从头测序技术的发明者,在从头测序领域有20多年的经验积累。目前,我们的标准程序结合了自上而下和自下而上的质谱技术,确保了每一个氨基酸的正确性和全抗体的序列精度,包括末端及C末端的修饰和N-连接的聚糖,可弥补传统蛋白质鉴定方法在未知蛋白质序列和突变分析上的不足。
参考文献:
1. de Graaf SC, Hoek M, Tamara S, Heck AJR. A perspective toward mass spectrometry-based de novo sequencing of endogenous antibodies. MAbs. 2022 Jan-Dec;14(1):2079449.
2. Bondt A, Hoek M, Tamara S, de Graaf B, Peng W, Schulte D, van Rijswijck DMH, den Boer MA, Greisch JF, Varkila MRJ, Snijder J, Cremer OL, Bonten MJM, Heck AJR. Human plasma IgG1 repertoires are simple, unique, and dynamic. Cell Syst. 2021 Dec 15;12(12):1131-1143.